Aby pobrać lub wydrukować tę stronę w innym języku, wybierz najpierw swój język z menu rozwijanego w lewym górnym rogu.

Stanowisko IAOMT w sprawie kawitacji ludzkiej kości szczęki
Przewodniczący Komisji Patologii Kości Jawbone: Ted Reese, DDS, MAGD, NMD, FIAOMT
Karl Anderson, DDS, MS, NMD, FIAOMT
Patricia Berube, DMD, MS, CFMD, FIAOMT
Jerry Bouquot, DDS, MSD
Teresa Franklin, dr hab
Jack Kall, DMD, FAGD, MIAOMT
Cody Kriegel, DDS, NMD, FIAOMT
Sushma Lavu, DDS, FIAOMT
Tiffany Shields, DMD, NMD, FIAOMT
Marek Wiśniewski, DDS, FIAOMT
Komisja pragnie wyrazić nasze uznanie Michaelowi Gossweilerowi, DDS, MS, NMD, Miguelowi Stanleyowi, DDS i Stuartowi Nunally, DDS, MS, FIAOMT, NMD za ich krytykę tego artykułu. Pragniemy również wyrazić uznanie dla nieocenionego wkładu i wysiłku dr Nunnally’ego w opracowanie stanowiska za rok 2014. Jego praca, pracowitość i praktyka stały się podstawą tego zaktualizowanego artykułu.
Zatwierdzony przez Radę Dyrektorów IAOMT we wrześniu 2023 r
Spis treści
Tomografia komputerowa wiązki stożkowej (CBCT)
Biomarkery i badanie histologiczne
Ewoluujące rozważania do celów diagnostycznych
Implikacje systemowe i kliniczne
Alternatywne strategie leczenia
Referencje
Dodatek I Wyniki ankiety IAOMT 2
Dodatek II Wyniki ankiety IAOMT 1
Dodatek III Obrazy
Rycina 1. Tłuszczowa zwyrodnieniowa martwica kości szczęki (FDOJ)
Rycina 2 Cytokiny w FDOJ w porównaniu ze zdrowymi kontrolami
Rycina 3. Zabieg chirurgiczny w przypadku retromolarnego FDOJ
Rycina 4 Łyżeczkowanie i odpowiednie prześwietlenie FDOJ
Filmy Klipy wideo przedstawiające operacje kości szczęki u pacjentów
W ciągu ostatniej dekady wśród społeczeństwa i podmiotów świadczących opiekę zdrowotną wzrosła świadomość związku pomiędzy zdrowiem jamy ustnej a zdrowiem ogólnoustrojowym. Na przykład choroba przyzębia jest czynnikiem ryzyka zarówno cukrzycy, jak i chorób serca. Wykazano także potencjalnie istotny i coraz częściej badany związek pomiędzy patologią kości szczęki a ogólnym stanem zdrowia i witalnością jednostki. Zastosowanie zaawansowanych technicznie metod obrazowania, takich jak tomografia komputerowa wiązki stożkowej (CBCT), odegrało zasadniczą rolę w identyfikacji patologii kości szczęki, co doprowadziło do poprawy możliwości diagnostycznych i lepszej oceny powodzenia interwencji chirurgicznych. Doniesienia naukowe, dramaty dokumentalne i media społecznościowe zwiększyły świadomość społeczną na temat tych patologii, szczególnie wśród osób cierpiących na niewyjaśnione przewlekłe schorzenia neurologiczne lub ogólnoustrojowe, które nie reagują na tradycyjne interwencje medyczne lub stomatologiczne.
Międzynarodowa Akademia Medycyny Jamy Ustnej i Toksykologii (IAOMT) opiera się na przekonaniu, że nauka powinna być podstawą wyboru i wykorzystania wszystkich metod diagnostycznych i leczniczych. Mając ten priorytet na uwadze, 1) przedstawiamy tę aktualizację naszego dokumentu przedstawiającego stanowisko IAOMT Jawbone Osteonecrosis z 2014 r. oraz 2) proponujemy, w oparciu o obserwacje histologiczne, bardziej dokładną z naukowego i medycznego punktu widzenia nazwę choroby, w szczególności przewlekłą niedokrwienną chorobę rdzeniastą kości szczęki (CIMDJ). CIMDJ opisuje stan kości charakteryzujący się śmiercią składników komórkowych kości gąbczastej, wtórną do przerwania dopływu krwi. W całej swojej historii to, co nazywamy CIMDJ, było określane wieloma nazwami i akronimami, które wymieniono w tabeli 1 i zostaną pokrótce omówione poniżej.
Celem i intencją tej Akademii oraz artykułu jest udostępnienie danych naukowych, badań i obserwacji klinicznych pacjentom i klinicystom, aby mogli podejmować świadome decyzje dotyczące zmian CIMDJ, często określanych jako kawitacje kości szczęki. Artykuł z 2023 r. powstał wspólnym wysiłkiem klinicystów, badaczy i wybitnego patologa kości szczęki, dr Jerry'ego Bouquot, po przejrzeniu ponad 270 artykułów.
W żadnej innej kości ryzyko urazów i infekcji nie jest tak duże, jak w przypadku kości szczęki. Przegląd literatury dotyczącej kawitacji kości szczęki (tj. CIMDJ) pokazuje, że schorzenie to jest diagnozowane, leczone i badane od lat sześćdziesiątych XIX wieku. W 1860 roku dr HR Noel wygłosił prezentację pt Wykład na temat próchnicy i martwicy kości w Baltimore College of Dental Surgery, a w 1901 roku William C. Barrett szczegółowo omówił kawitacje kości szczęki w jego podręczniku zatytułowanym Oral Pathology and Practice: A Textbook for the Use of Students in Dental Colleges and a Handbook for Dental Practitioners. GV Black, często nazywany ojcem współczesnej stomatologii, w swoim podręczniku Special Dental Pathology z 1915 r. zamieścił rozdział opisujący „zwykły wygląd i leczenie” tego, co określił jako martwica kości szczęki (JON).
Wydawało się, że badania nad kawitacją kości szczęki ustały aż do lat 1970. XX wieku, kiedy inni zaczęli zgłębiać ten temat, używając różnych nazw i etykiet oraz publikując informacje na ten temat we współczesnych podręcznikach patologii jamy ustnej. Na przykład w 1992 roku Bouquot i wsp. zaobserwowali śródkostne zapalenie u pacjentów z przewlekłym i silnym bólem twarzy (N=135) i ukuli termin „Neuralgia-inducing Cavitational Osteonecrosis” (NICO). Chociaż Bouquot i wsp. nie skomentowali etiologii choroby, doszli do wniosku, że prawdopodobne jest, że zmiany wywołały przewlekłą neuralgię twarzy o unikalnych cechach lokalnych: tworzeniu się jamy śródkostnej i długotrwałej martwicy kości z minimalnym gojeniem. W badaniu klinicznym pacjentów z neuralgią nerwu trójdzielnego (N=38) i nerwu twarzowego (N=33) Ratner i wsp. również wykazali, że prawie wszyscy pacjenci mieli ubytki w kości wyrostka zębodołowego i kości szczęki. Ubytki, czasami o średnicy większej niż 1 centymetr, znajdowały się w miejscach poprzednich ekstrakcji zębów i na ogół nie były wykrywalne za pomocą promieni rentgenowskich.

 W literaturze istnieje wiele innych terminów określających to, co identyfikujemy jako CIMDJ. Wymieniono je w tabeli 1 i pokrótce omówiono tutaj. Adams i wsp. w swoim stanowisku z 2014 r. ukuli termin „przewlekłe włókniające zapalenie kości i szpiku” (CFO). Stanowisko powstało w wyniku prac multidyscyplinarnego konsorcjum lekarzy z dziedzin medycyny jamy ustnej, endodoncji, patologii jamy ustnej, neurologii, reumatologii, otolaryngologii, periodontologii, psychiatrii, radiologii jamy ustnej i szczękowo-twarzowej, anestezjologii, stomatologii ogólnej, chorób wewnętrznych i leczenia bólu. . Celem grupy było zapewnienie interdyscyplinarnej platformy do leczenia schorzeń głowy, szyi i twarzy. Dzięki zbiorowym wysiłkom tej grupy, obszernym przeszukiwaniom literatury i wywiadom z pacjentami wyłonił się odrębny wzór kliniczny, który nazwali dyrektorem finansowym. Zauważyli, że choroba ta często pozostaje niezdiagnozowana ze względu na współistnienie z innymi schorzeniami ogólnoustrojowymi. Grupa ta zwróciła uwagę na potencjalne powiązania choroby z ogólnoustrojowymi problemami zdrowotnymi oraz na potrzebę posiadania zespołu lekarzy w celu prawidłowego zdiagnozowania i leczenia pacjenta.
W literaturze istnieje wiele innych terminów określających to, co identyfikujemy jako CIMDJ. Wymieniono je w tabeli 1 i pokrótce omówiono tutaj. Adams i wsp. w swoim stanowisku z 2014 r. ukuli termin „przewlekłe włókniające zapalenie kości i szpiku” (CFO). Stanowisko powstało w wyniku prac multidyscyplinarnego konsorcjum lekarzy z dziedzin medycyny jamy ustnej, endodoncji, patologii jamy ustnej, neurologii, reumatologii, otolaryngologii, periodontologii, psychiatrii, radiologii jamy ustnej i szczękowo-twarzowej, anestezjologii, stomatologii ogólnej, chorób wewnętrznych i leczenia bólu. . Celem grupy było zapewnienie interdyscyplinarnej platformy do leczenia schorzeń głowy, szyi i twarzy. Dzięki zbiorowym wysiłkom tej grupy, obszernym przeszukiwaniom literatury i wywiadom z pacjentami wyłonił się odrębny wzór kliniczny, który nazwali dyrektorem finansowym. Zauważyli, że choroba ta często pozostaje niezdiagnozowana ze względu na współistnienie z innymi schorzeniami ogólnoustrojowymi. Grupa ta zwróciła uwagę na potencjalne powiązania choroby z ogólnoustrojowymi problemami zdrowotnymi oraz na potrzebę posiadania zespołu lekarzy w celu prawidłowego zdiagnozowania i leczenia pacjenta.
U dzieci obserwowano także zmiany kawitacyjne kości szczęki. W 2013 roku Obel i wsp. opisali zmiany chorobowe u dzieci i ukuli termin młodzieńcze przewlekłe zapalenie kości i szpiku żuchwy (JMCO). Grupa ta zasugerowała możliwość zastosowania dożylnych (IV) bisfosfonianów w leczeniu tych dzieci. W 2016 roku Padwa i wsp. opublikowali badanie opisujące ogniskowe jałowe zapalenie kości w kościach szczęk u dzieci i młodzieży. Nazwali zmianę „Przewlekłe niebakteryjne zapalenie kości i szpiku u dzieci” (CNO).
Od 2010 roku dr Johann Lechner, autor i badacz najszerzej publikowanych publikacji na temat uszkodzeń kawitacyjnych kości szczęki, oraz inni badacze badają związek tych zmian z produkcją cytokin, zwłaszcza cytokiny zapalnej RANTES (znanej również jako CCL5). Doktor Lechner użył różnych terminów do opisania tych zmian, do których zalicza się wspomnianą wcześniej NICO, ale także aseptyczną niedokrwienną martwicę kości szczęki (AIOJ) i tłuszczową zwyrodnieniową martwicę kości szczęki (FDOJ). Jego opis/etykieta opiera się na wyglądzie fizycznym i/lub makroskopowo stanie patologicznym obserwowanym klinicznie lub śródoperacyjnie.
Istnieje obecnie potrzeba wyjaśnienia innej, niedawno zidentyfikowanej patozy kości szczęki, która różni się od tematu tego artykułu, ale może być myląca dla badaczy zmian kawitacyjnych. Są to zmiany kostne szczęki, które powstają na skutek stosowania środków farmaceutycznych. Zmiany najlepiej charakteryzują się utratą dopływu krwi i następczą niekontrolowaną sekwestracją kości. Zmiany te zostały nazwane przez Ruggiero i wsp. owrzodzeniem jamy ustnej z sekwestracją kości (OUBS) w dokumencie pt. Amerykańskie Stowarzyszenie Chirurgów Szczękowo-Twarzowych (AAOMS), a także Palla i wsp. w przeglądzie systematycznym. Ponieważ problem ten jest związany ze stosowaniem jednego lub wielu leków, IAOMT stoi na stanowisku, że tego typu zmiany najlepiej opisać jako martwicę kości szczęki związaną z lekami (MRONJ). MRONJ nie będzie omawiany w tym artykule, ponieważ jego etiologia i metody leczenia różnią się od tego, co nazywamy CIMDJ, i było ono wcześniej szeroko badane.
Coraz powszechniejsze stosowanie przez wielu lekarzy dentystów zdjęć rentgenowskich tomografii komputerowej wiązki stożkowej (CBCT) doprowadziło do wzrostu liczby pacjentów obserwujących kawitacje śródszpikowe, które nazywamy CIMDJ, a które wcześniej były pomijane i dlatego ignorowane. Teraz, gdy te zmiany i anomalie są łatwiej identyfikowane, obowiązkiem lekarzy dentystów jest zdiagnozowanie choroby oraz zapewnienie zaleceń dotyczących leczenia i opieki.
Docenienie i identyfikacja istnienia CIMDJ jest punktem wyjścia do jego zrozumienia. Niezależnie od wielu nazw i akronimów kojarzonych z tą patologią, obecność martwicy lub obumierania kości w szpiku kostnym szczęki jest dobrze potwierdzona.
Jeśli te defekty kostne zostaną zaobserwowane podczas operacji, mogą one objawiać się na wiele sposobów. Niektórzy praktycy podają, że ponad 75% zmian jest całkowicie pustych lub wypełnionych miękką, szarobrązową i zdemineralizowaną tkanką/ziarniniakiem, często z żółtym oleistym materiałem (cysty olejowe) znajdującym się w uszkodzonych obszarach z otaczającą normalną anatomią kości. Inni zgłaszają obecność kawitacji o różnej gęstości leżącej nad nimi kości korowej, które po otwarciu wydają się mieć wyściółkę z włóknistych czarnych, brązowych lub szarych materiałów nitkowatych. Jeszcze inni donoszą o dużych zmianach, określanych różnie jako „zapiaszczone”, „przypominające trociny”, „puste ubytki” i „suche”, z okazjonalną sklerotyczną twardością ścian ubytku przypominającą zęby. W badaniu histologicznym zmiany te wydają się podobne do martwicy występującej w innych kościach ciała i histologicznie różnią się od zapalenia kości i szpiku (patrz ryc. 1). Dodatkowe obrazy ilustrujące chorobę CIMDJ, niektóre o charakterze graficznym, znajdują się w Załączniku III na końcu tego dokumentu.
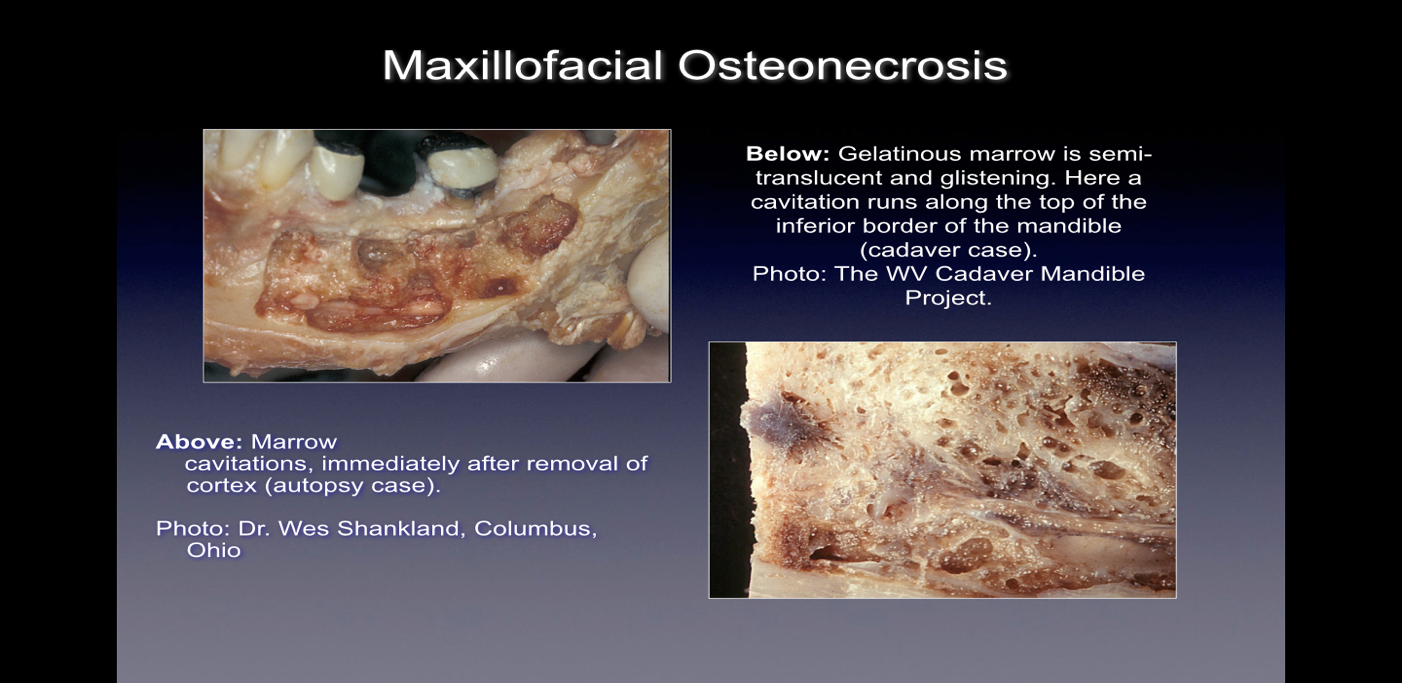
Rysunek 1 Zdjęcia CIMDJ pobrane ze zwłok
Podobnie jak inni pracownicy służby zdrowia, dentyści stosują zorganizowany proces, który wykorzystuje różne metody i sposoby diagnozowania uszkodzeń kawitacyjnych. Mogą one polegać na przeprowadzeniu badania przedmiotowego, które obejmuje zebranie wywiadu, ocenę objawów, pobranie płynów ustrojowych w celu przeprowadzenia badań laboratoryjnych oraz pobranie próbek tkanek do biopsji i badań mikrobiologicznych (tj. badania na obecność patogenów). Często stosowane są również technologie obrazowania, takie jak CBCT. U pacjentów ze złożonymi zaburzeniami, które nie zawsze układają się według określonego schematu lub mieszczą się w typowym porządku zespołu objawów, proces diagnostyczny może wymagać bardziej szczegółowej analizy, która początkowo może skutkować jedynie rozpoznaniem różnicowym. Poniżej przedstawiono krótki opis kilku z tych metod diagnostycznych.
Tomografia komputerowa wiązki stożkowej (CBCT)
W diagnostyce kawitacji kości szczęki przydatne są techniki diagnostyczne opisane już w 1979 roku przez Ratnera i współpracowników, wykorzystujące palpację i naciski palców, diagnostyczne zastrzyki środków znieczulających miejscowo, uwzględnienie wywiadu chorobowego i lokalizację bólu promieniującego. Jednakże, chociaż niektóre z tych zmian powodują ból, obrzęk, zaczerwienienie, a nawet gorączkę, inne nie. Dlatego często konieczny jest bardziej obiektywny środek, taki jak obrazowanie.
Kawitacji zwykle nie wykrywa się na standardowych dwuwymiarowych (2D, np. okołowierzchołkowych i panoramicznych) kliszach radiograficznych, które są powszechnie stosowane w stomatologii. Ratner i współpracownicy wykazali, że co najmniej 40% kości wymaga zmiany, aby uwidocznić zmiany, co potwierdzają późniejsze prace i co zilustrowano na rycinie 2. Jest to związane z nieodłącznym ograniczeniem obrazowania 2D, które powoduje nakładanie się struktur anatomicznych, maskując obszary zainteresowania. W przypadku ubytków lub patologii, szczególnie w obrębie żuchwy, efekt maskowania gęstej kości korowej na leżących pod nią strukturach może być znaczący. Dlatego wymagane są zaawansowane technologicznie techniki obrazowania, takie jak CBCT, tomografia Tech 99, rezonans magnetyczny (MRI) czy ultrasonografia przezpęcherzykowa (CaviTAU™®).
Spośród różnych dostępnych technik obrazowania, CBCT jest najpowszechniej stosowanym narzędziem diagnostycznym stosowanym przez dentystów zajmujących się diagnozowaniem lub leczeniem kawitacji i dlatego zostanie omówione szczegółowo. Podstawą technologii CBCT jest możliwość oglądania interesującej zmiany chorobowej w 3 wymiarach (czołowym, strzałkowym, czołowym). CBCT okazało się niezawodną i dokładną metodą identyfikacji i szacowania wielkości i zasięgu ubytków śródkostnych w szczęce przy mniejszych zniekształceniach i mniejszym powiększeniu niż zdjęcia rentgenowskie 2D.
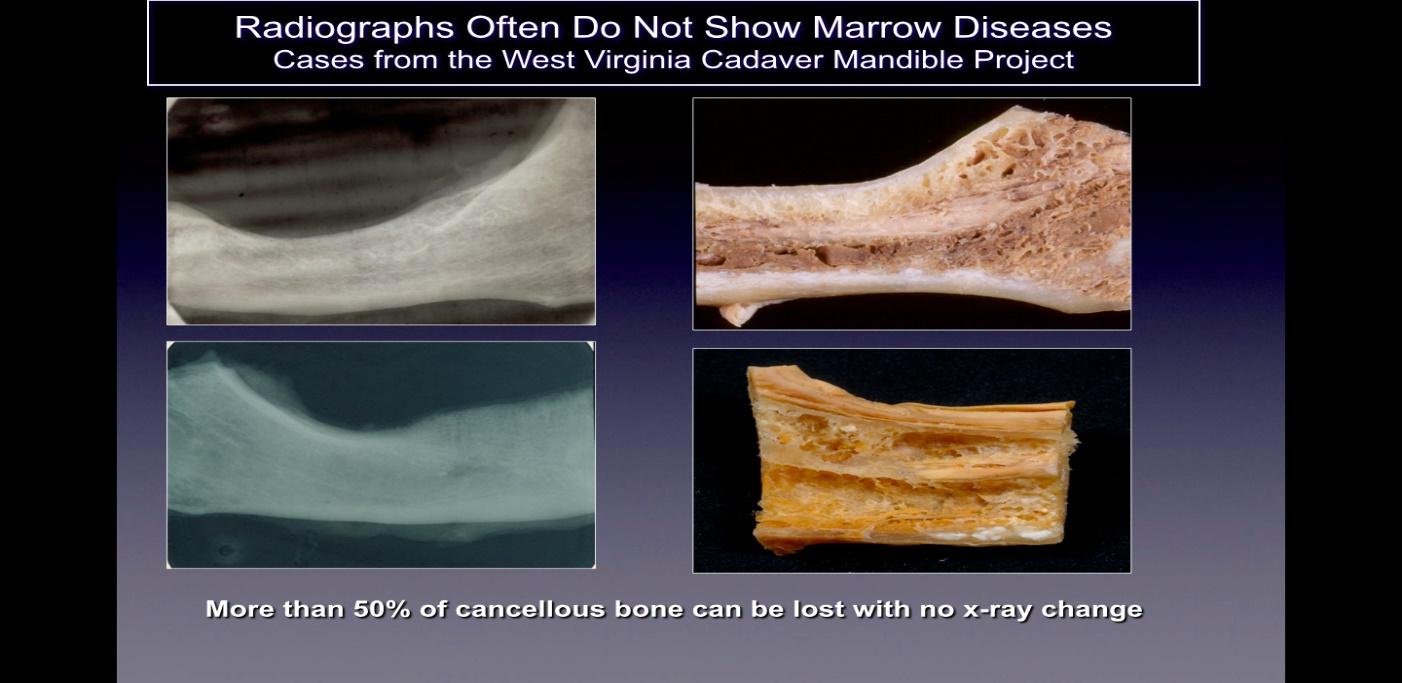
Rysunek 2 Podpis: Po lewej stronie pokazano radiogramy 2D kości szczęk pobranych ze znalezionych zwłok
zdrowy. Po prawej stronie figury znajdują się fotografie tych samych kości szczęk, na których widać wyraźną kawitację martwiczą.
Rysunek na podstawie Bouquot, 2014.
Badania kliniczne wykazały, że obrazy CBCT pomagają również w określeniu zawartości zmiany (wypełnionej płynem, ziarniniakowej, litej itp.), co może pomóc w rozróżnieniu zmian zapalnych, guzów zębopochodnych i niezębogennych, torbieli i innych łagodnych lub złośliwych zmian. uszkodzenia .
Niedawno opracowane oprogramowanie, specjalnie zintegrowane z różnymi typami urządzeń CBCT, wykorzystuje jednostki Hounsfielda (HU), co pozwala na standaryzowaną ocenę gęstości kości. HU reprezentuje względną gęstość tkanek ciała według skalibrowanej skali szarości, opartej na wartościach dla powietrza (-1000 HU), wody (0 HU) i gęstości kości (+1000 HU). Rycina 3 przedstawia różne widoki współczesnego obrazu CBCT.
Podsumowując, CBCT okazało się przydatne w diagnostyce i leczeniu kawitacji kości szczęki poprzez:
- Identyfikacja rozmiaru, zasięgu i położenia 3-D zmiany chorobowej;
- Identyfikacja bliskości zmiany chorobowej do innych pobliskich ważnych struktur anatomicznych, takich jak
nerw zębodołowy dolny, zatoka szczękowa lub sąsiadujące korzenie zębów;
- Określenie podejścia do leczenia: chirurgiczne czy niechirurgiczne; I
- Dostarczenie obrazu kontrolnego w celu określenia stopnia zagojenia i ewentualnej potrzeby
aby ponownie wyleczyć zmianę.
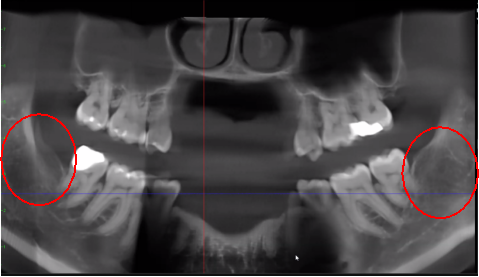
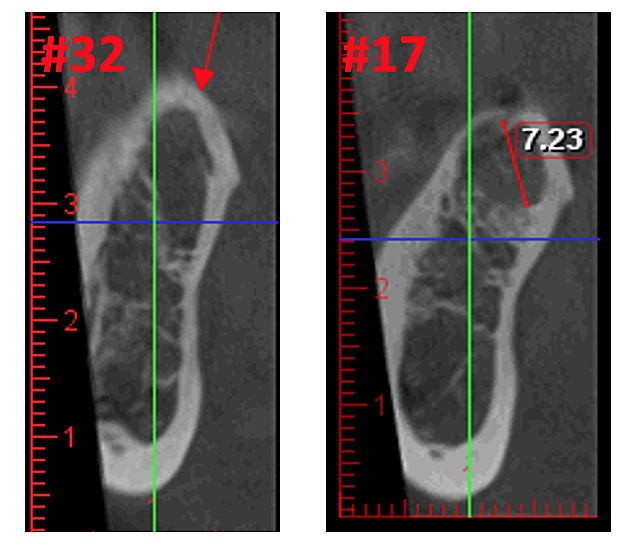
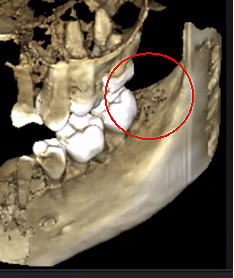
Rysunek 3 Większa przejrzystość obrazu CBCT dzięki udoskonalonej technologii oprogramowania, która redukuje artefakty i „szumy”, które mogą powodować na obrazie implanty dentystyczne i uzupełnienia metalowe. Dzięki temu dentysta i pacjent mogą łatwiej zwizualizować zmianę. Górny panel przedstawia panoramiczny widok CBCT pokazujący lewą (#17) i prawą (#32) lokalizację i zasięg zmian kawitacyjnych u pacjenta z martwicą kości szczęki. Lewy dolny panel przedstawia widok strzałkowy każdego miejsca. Prawy dolny panel to trójwymiarowa wizualizacja miejsca nr 3 przedstawiająca porowatość korową leżącą nad kawitacją rdzeniową. Dzięki uprzejmości doktora Reese.
W tym miejscu krótko wspominamy także o urządzeniu ultradźwiękowym CaviTAU™®, które zostało opracowane i jest stosowane w niektórych częściach Europy, szczególnie do wykrywania obszarów o małej gęstości kości w górnej i dolnej szczęce, które sugerują kawitację kości szczęki. To przezpęcherzykowe urządzenie do ultrasonografii ultradźwiękowej (TAU-n) jest potencjalnie porównywalne z CBCT pod względem wykrywania uszkodzeń szpiku kostnego szczęki, a jego dodatkową zaletą jest narażenie pacjenta na znacznie niższe poziomy promieniowania. Urządzenie to jest obecnie niedostępne w USA, ale jest poddawane przeglądowi przez amerykańską Agencję ds. Żywności i Leków i może równie dobrze być głównym narzędziem diagnostycznym stosowanym w Ameryce Północnej w leczeniu CIMJD.
Biomarkery i badanie histologiczne
Ze względu na zapalny charakter ubytków kości szczęki Lechner i Baehr w 2017 roku zbadali możliwy związek między wybranymi cytokinami a chorobą. Jedna cytokina będąca przedmiotem szczególnego zainteresowania podlega „regulacji po aktywacji, ekspresji i wydzielaniu normalnych limfocytów T” (RANTES). Cytokina ta, podobnie jak czynnik wzrostu fibroblastów (FGF)-2, ulega ekspresji w większych ilościach w zmianach kawitacyjnych i u pacjentów z CIMDJ. Rycina 4, dostarczona przez dr Lechnera, porównuje poziomy RANTES u pacjentów z kawitacją (czerwony słupek po lewej) z poziomami u zdrowych osób w grupie kontrolnej (niebieski słupek), wykazując poziomy ponad 25 razy wyższe u osób z tą chorobą. Lechner i wsp. stosują dwa podejścia do pomiaru poziomów cytokin. Jednym z nich jest ogólnoustrojowy pomiar poziomu cytokin we krwi (Laboratorium Rozwiązań Diagnostycznych, USA.). Drugą metodą jest pobranie biopsji bezpośrednio z miejsca objętego chorobą, po uzyskaniu dostępu do niej w celu oceny przez patologa jamy ustnej. Niestety, obecnie zlokalizowane pobieranie próbek tkanek wymaga złożonego przetwarzania i transportu, czego nie udało się jeszcze osiągnąć w placówkach innych niż badawcze, ale dostarczyło wnikliwych korelacji.
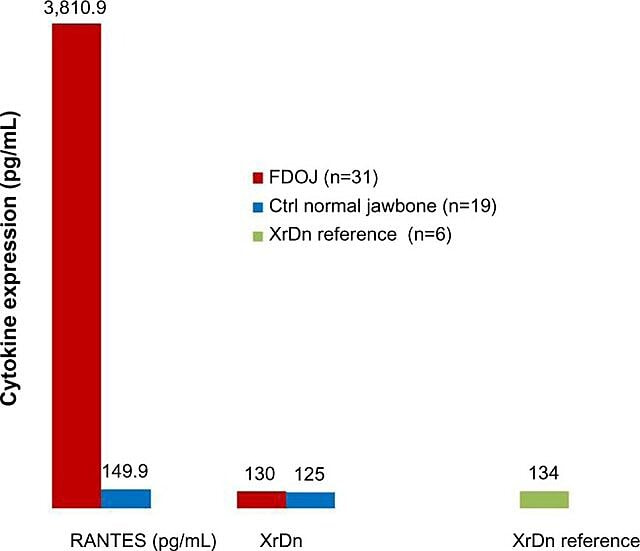
Rysunek 4 Rozkład RANTES w 31 przypadkach FDOJ i 19 próbkach prawidłowej kości szczęki w porównaniu z referencyjną gęstością promieniowania rentgenowskiego dla obu grup w odpowiednich obszarach. Skróty: RANTES, regulowany po aktywacji, ligand 5 normalnej chemokiny wyrażanej i wydzielanej przez komórki T (motyw CC); XrDn, gęstość promieniowania rentgenowskiego; FDOJ, tłuszczowa zwyrodnieniowa martwica kości szczęki; n, liczba; Ctrl, kontrola. Rysunek udostępniony przez dr Lechnera. Numer licencji: CC BY-NC 3.0
Ewoluujące rozważania do celów diagnostycznych
Obecność kawitacji kości szczęki została dobrze potwierdzona klinicznie. Jednak jasne diagnozy i parametry leczenia oparte na najlepszych praktykach wymagają dalszych badań. Mając to na uwadze, należy pokrótce wspomnieć o kilku intrygujących i potencjalnie wartościowych technikach, z których korzystają niektórzy praktycy.
Uznaje się, że dodatkowe badania fizjologiczne byłyby cennym narzędziem przesiewowym i diagnostycznym. Jednym z takich narzędzi, z którego korzystają niektórzy praktycy, jest obrazowanie termowizyjne. Uogólnioną aktywność zapalną można zaobserwować mierząc różnicę ciepła na powierzchni głowy i szyi. Termografia jest metodą bezpieczną, szybką i może mieć wartość diagnostyczną podobną do CBCT. Istotną wadą jest brak definicji, co utrudnia określenie marginesu lub zasięgu zmiany.
Niektórzy praktycy przyglądają się profilowi energetycznemu zmiany chorobowej, wykorzystując ocenę meridianów akupunktury (AMA) w celu określenia jej wpływu na odpowiadający jej meridian energetyczny. Ten rodzaj oceny opiera się na elektroakupunkturze według Volla (EAV). Technika ta, oparta na starożytnej medycynie chińskiej i zasadach akupunktury, została opracowana i jest nauczana w USA. Akupunkturę stosowano w celu łagodzenia bólu i wspomagania gojenia. Opiera się na równowadze przepływu energii (tj. Chi) przez określone ścieżki energetyczne w organizmie. Te ścieżki, czyli meridiany, łączą ze sobą określone narządy, tkanki, mięśnie i kości. Akupunktura wykorzystuje bardzo specyficzne punkty na meridianie, aby wpłynąć na zdrowie i witalność wszystkich elementów ciała znajdujących się na tym meridianie. Technikę tę zastosowano do wykrycia choroby kości szczęki, która po wyleczeniu leczy również pozornie niezwiązane ze sobą choroby, takie jak zapalenie stawów lub zespół chronicznego zmęczenia. Technika ta nadaje się do dalszych badań (tzn. należy udokumentować wyniki oraz pozyskać i rozpowszechnić dane podłużne).
Istnieje wiele indywidualnych czynników, które zwiększają ryzyko rozwoju kawitacji kości szczęki, ale zazwyczaj ryzyko jest wieloczynnikowe. Zagrożenia dla jednostki mogą wynikać z czynników zewnętrznych, takich jak czynniki środowiskowe, lub czynników wewnętrznych, takich jak słaba funkcja odpornościowa. W tabelach 2 i 3 zestawiono zewnętrzne i wewnętrzne czynniki ryzyka.


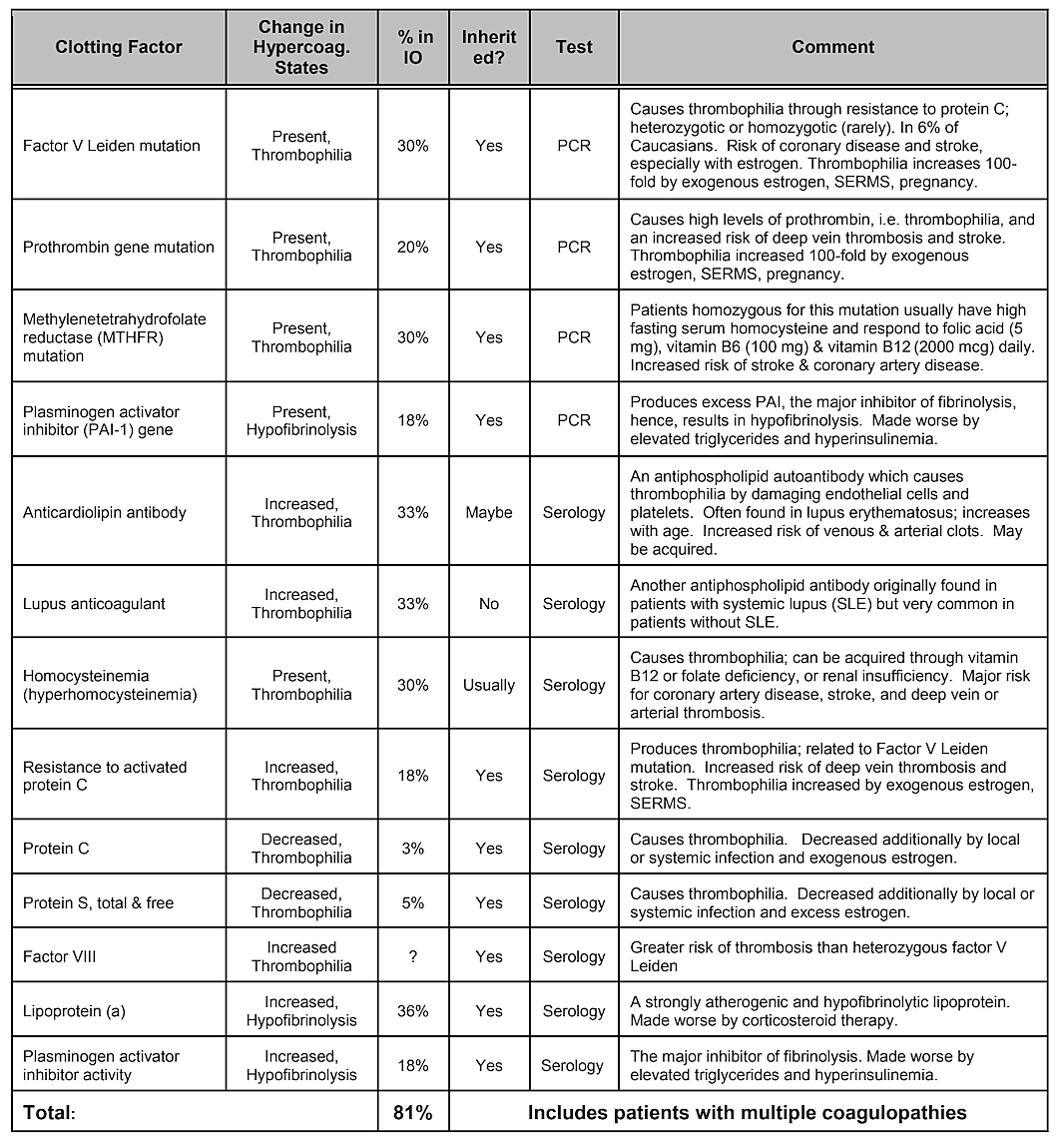
Należy zauważyć, że Tabela 2, Wewnętrzne czynniki ryzyka, nie uwzględnia predyspozycji genetycznych. Chociaż uważa się, że wariancje genetyczne odgrywają pewną rolę, nie wykazano, aby pojedyncza odmiana genu lub nawet kombinacja genów została zidentyfikowana jako czynnik ryzyka, chociaż prawdopodobne są wpływy genetyczne . Systematyczny przegląd literatury przeprowadzony w 2019 r. wykazał, że zidentyfikowano szereg polimorfizmów pojedynczych nukleotydów, ale nie ma replikacji między badaniami. Autorzy doszli do wniosku, że biorąc pod uwagę różnorodność genów, które wykazały pozytywne powiązania z kawitacją oraz brak powtarzalności badań, rola przyczyn genetycznych wydaje się umiarkowana i niejednorodna. Jednakże w celu zidentyfikowania różnic genetycznych konieczne może być skierowanie badań na określone populacje. Rzeczywiście, jak wykazano, jednym z najczęstszych i podstawowych mechanizmów patofizjologicznych niedokrwiennego uszkodzenia kości jest nadmierne krzepnięcie spowodowane stanami hiperkoagulacji, które zwykle mają podłoże genetyczne, jak opisali Bouquot i Lamarche (1999). Tabela 4 dostarczona przez dr Bouquot zawiera listę stanów chorobowych związanych z nadkrzepliwością, a kolejne 3 akapity zawierają przegląd niektórych odkryć dr Bouquot, które przedstawił jako dyrektor ds. badań w Centrum Edukacji i Badań Szczękowo-Twarzowych.
W przypadku kawitacji kości szczęki występują wyraźne objawy niedokrwiennej martwicy kości, czyli choroby szpiku kostnego, w której kość staje się martwicza z powodu niedoboru tlenu i składników odżywczych. Jak wspomniano, wiele czynników może oddziaływać na siebie, powodując kawitację, a nawet 80% pacjentów ma problem, zwykle dziedziczny, polegający na nadmiernym tworzeniu się skrzepów krwi w naczyniach krwionośnych. Ta choroba zwykle nie jest wykrywana podczas rutynowych badań krwi. Kości są szczególnie podatne na problem nadkrzepliwości i rozwijają się w nich znacznie rozszerzone naczynia krwionośne; zwiększone, często bolesne ciśnienie wewnętrzne; stagnacja krwi; a nawet zawał. Na ten problem związany z nadkrzepliwością może sugerować występowanie w rodzinie udarów i zawałów serca we wczesnym wieku (poniżej 55 lat), wymiany stawu biodrowego lub „artretyzmu” (szczególnie we wczesnym wieku), martwicy kości (szczególnie we wczesnym wieku), głębokiej zakrzepica żył, zatorowość płucna (skrzepy krwi w płucach), zakrzepica żył siatkówki (skrzepy w siatkówce oka) i nawracające poronienia. W przypadku tej choroby szczęki mają dwa specyficzne problemy: 2) uszkodzona, chora kość jest słabo odporna na infekcje o niskim stopniu nasilenia wywołane bakteriami zębów i dziąseł; oraz 1) kość może nie zregenerować się po zmniejszonym przepływie krwi wywołanym przez miejscowe środki znieczulające stosowane przez dentystów podczas prac stomatologicznych. Rycina 2 przedstawia obraz mikroskopowy skrzepliny wewnątrznaczyniowej.
Tabela 4 Stany chorobowe obejmujące nadkrzepliwość. U czterech na pięciu pacjentów z kawitacją kości szczęki występuje takie krzepnięcie
problemy czynnikowe.
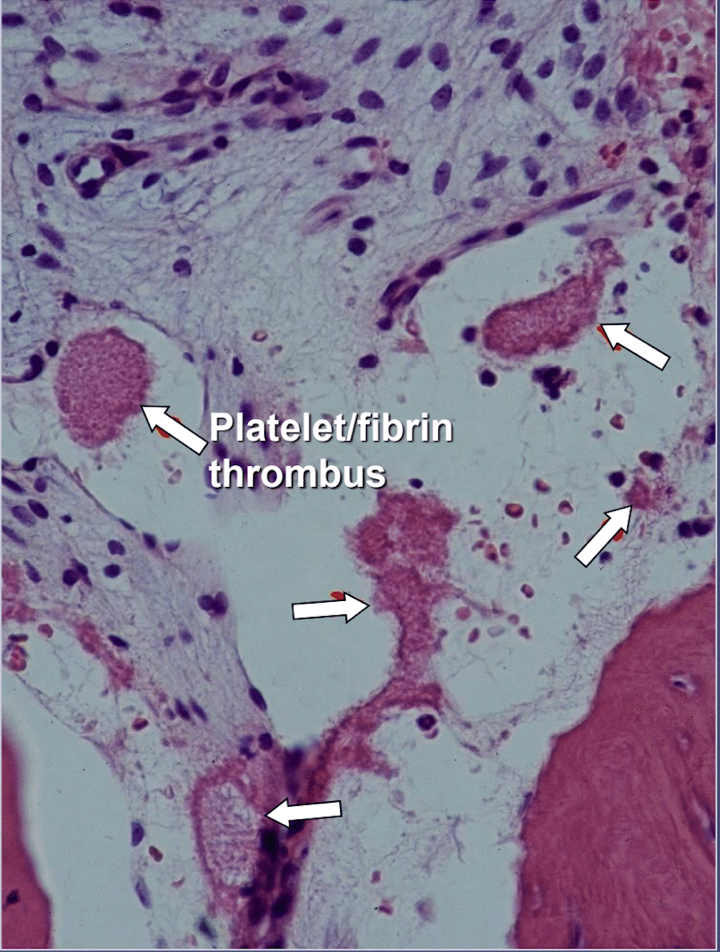
Niezależnie od przyczyny hiperkoagulacji, w kości rozwija się szpik włóknisty (włókna mogą żyć w obszarach ubogich w składniki odżywcze), tłusty, martwy szpik tłuszczowy („mokra zgnilizna”), bardzo suchy, czasami skórzasty szpik („sucha zgnilizna”) ) lub całkowicie pustą przestrzeń szpikową („kawitacja”).
Zajęta może być każda kość, jednak najczęściej zajęte są biodra, kolana i szczęki. Ból jest często silny, ale wynosi około 1/3rd pacjentów nie odczuwa bólu. Organizm ma problemy z wyleczeniem się z tej choroby i 2/3rds przypadków wymaga chirurgicznego usunięcia uszkodzonego szpiku, zwykle poprzez zeskrobanie łyżeczką. Operacja wyeliminuje problem (i ból) za prawie 3/4ths pacjentów z zajęciem szczęki, chociaż u 40% pacjentów wymagane są powtórne operacje, zwykle mniejsze niż pierwsze, czasami w innych częściach szczęki, ponieważ w chorobie często występują zmiany „przeskakujące” (tj. takie same lub podobne kości), z normalnym szpikiem pomiędzy. Ponad połowa pacjentów z biodrem ostatecznie zachoruje na przeciwległy staw biodrowy. Ponad 1/3rd pacjentów z kością szczęki zaatakuje inne ćwiartki szczęki. Niedawno odkryto, że u 40% pacjentów z martwicą kości biodra lub szczęki odpowiedź na leczenie przeciwzakrzepowe heparyną drobnocząsteczkową (Lovenox) lub kumadyną powoduje ustąpienie bólu i gojenie kości.
Rysunek 5 Obraz mikroskopowy skrzeplin wewnątrznaczyniowych
Jeśli poszukuje się niefarmaceutycznego podejścia w celu zmniejszenia ryzyka nadkrzepliwości, można rozważyć zastosowanie dodatkowych enzymów, takich jak nattokinaza lub silniejsza lumbrokinaza, z których oba mają właściwości fibrynolityczne i przeciwzakrzepowe. Ponadto należy wykluczyć stany niedoboru miedzi, które mogą wiązać się z zaburzeniami krzepnięcia, ze względu na zwiększone ryzyko wystąpienia nadkrzepliwości obserwowane u pacjentów z kawitacją kości szczęki.
IMPLIKACJE SYSTEMOWE I KLINICZNE
Obecność kawitacji kości szczęki i związana z nią patologia obejmują pewne specyficzne objawy, ale często obejmują także pewne niespecyficzne objawy ogólnoustrojowe. Dlatego zespół opiekuńczy powinien dokładnie rozważyć diagnozę i leczenie. Najbardziej unikalnymi i przełomowymi odkryciami, które wyszły na jaw od czasu stanowiska IAOMT 2014, jest rozwiązanie pozornie niezwiązanych ze sobą przewlekłych stanów zapalnych po leczeniu kawitacyjnym. Niezależnie od tego, czy choroby ogólnoustrojowe mają charakter autoimmunologiczny, czy też występuje inny stan zapalny, zgłaszano znaczną poprawę, w tym poprawę w zakresie raka. Zespół objawów związanych z tymi zmianami jest wysoce zindywidualizowany i dlatego nie można go uogólniać ani łatwo rozpoznawać. Dlatego też IAOMT stoi na stanowisku, że w przypadku zdiagnozowania u pacjenta kawitacji kości szczęki z towarzyszącym miejscowym bólem lub bez, a także u pacjenta występuje inna choroba ogólnoustrojowa, której wcześniej nie przypisywano kawitacji kości szczęki, pacjent wymaga dalszej oceny w celu ustalenia, czy choroba jest związana z lub jest konsekwencją choroby. IAOMT przeprowadziło ankietę wśród swoich członków, aby dowiedzieć się więcej o tym, jakie objawy/choroby ogólnoustrojowe ustępują po operacji kawitacyjnej. Wyniki przedstawiono w Załączniku I.
Wydaje się, że obecność cytokin wytwarzanych w słabo unaczynionych, martwiczych zmianach w kawitacjach kości szczęki funkcjonuje jako skupisko cytokin zapalnych, które utrzymują inne obszary zapalenia w stanie aktywnym i/lub przewlekłym. Oczekuje się złagodzenia lub przynajmniej poprawy miejscowego bólu szczęki po leczeniu, ale ta ogniskowa teoria stanu zapalnego, która zostanie szczegółowo omówiona poniżej, może wyjaśnić, dlaczego tak wiele pozornie „niepowiązanych” schorzeń, które mają związek z przewlekłymi stanami zapalnymi ulegają również zmniejszeniu w wyniku obróbki kawitacyjnej.
Na poparcie wniosków wyciągniętych ze stanowiska IAOMT z 2014 r. łączącego kawitację kości szczęki z chorobami ogólnoustrojowymi, badania i badania kliniczne opublikowane niedawno przez Lechnera, von Baehra i innych pokazują, że zmiany kawitacyjne kości szczęki zawierają specyficzny profil cytokin, niespotykany w innych patologiach kości . W porównaniu ze zdrowymi próbkami kości szczęki, patologie kawitacyjne stale wykazują silną regulację w górę czynnika wzrostu fibroblastów (FGF-2), antagonisty receptora interleukiny 1 (Il-1ra) i, co szczególnie ważne, RANTES. RANTES, znany również jako CCL5 (motyw cc Ligand 5), został opisany jako cytokina chemotaktyczna o silnym działaniu prozapalnym. Wykazano, że te chemokiny zakłócają kilka etapów odpowiedzi immunologicznej i są zasadniczo zaangażowane w różne stany patologiczne i infekcje. Badania wykazały, że RANTES ma związek z wieloma chorobami ogólnoustrojowymi, takimi jak zapalenie stawów, zespół chronicznego zmęczenia, atopowe zapalenie skóry, zapalenie nerek, zapalenie okrężnicy, łysienie, zaburzenia tarczycy oraz sprzyjanie stwardnieniu rozsianemu i chorobie Parkinsona. Ponadto wykazano, że RANTES powoduje przyspieszenie wzrostu nowotworu.
Czynniki wzrostu fibroblastów są również powiązane z kawitacją kości szczęki. Czynniki wzrostu fibroblastów, FGF-2 i związane z nimi receptory, są odpowiedzialne za wiele kluczowych funkcji, w tym proliferację, przeżycie i migrację komórek. Są również podatne na przejęcie przez komórki nowotworowe i odgrywają rolę onkogenną w wielu nowotworach. Na przykład FGF-2 sprzyja rozwojowi nowotworu i raka prostaty. Ponadto poziomy FGF-2 wykazały bezpośrednią korelację z progresją, przerzutami i złymi rokowaniami dotyczącymi przeżycia u pacjentów z rakiem jelita grubego. W porównaniu z grupą kontrolną wolną od nowotworu, pacjenci z rakiem żołądka mają znacznie wyższy poziom FGF-2 w surowicy. Te przekaźniki stanu zapalnego powiązano z wieloma poważnymi chorobami, niezależnie od tego, czy mają one charakter zapalny, czy nowotworowy. W przeciwieństwie do RANTES/CCL5 i FGF-2, wykazano, że IL1-ra działa jako silny mediator przeciwzapalny, przyczyniając się do braku powszechnych objawów zapalnych w obrębie niektórych zmian kawitacyjnych.
Nadmierne poziomy RANTES i FGF-2 w uszkodzeniach kawitacyjnych porównano i powiązano z poziomami obserwowanymi w innych chorobach ogólnoustrojowych, takich jak stwardnienie zanikowe boczne, (ALS), stwardnienie rozsiane (SM), reumatoidalne zapalenie stawów i rak piersi. Rzeczywiście, poziomy tych przekaźników wykrywane w kawitacjach kości szczęki są wyższe niż w surowicy i płynie mózgowo-rdzeniowym pacjentów z ALS i stwardnieniem rozsianym. Aktualne badania Lechnera i von Baehra wykazały 26-krotny wzrost RANTES w zmianach osteonekrotycznych kości szczęki u pacjentów z rakiem piersi. Lechner i współpracownicy sugerują, że RANTES uzyskany za pomocą kawitacji może przyspieszać rozwój i progresję raka piersi.
Jak wspomniano wcześniej, istnieje wiele przypadków bezobjawowych kawitacji kości szczęki. W tych przypadkach ostre cytokiny prozapalne, takie jak TNF-alfa i IL-6, NIE są obserwowane w zwiększonej liczbie w wynikach patohistologicznych próbek kawitacyjnych. U tych pacjentów brak tych cytokin prozapalnych jest związany z wysokim poziomem cytokiny przeciwzapalnej, antagonisty receptora interleukiny 1 (Il-1ra). Rozsądnym wnioskiem jest to, że ostry stan zapalny związany z kawitacją kości szczęki jest kontrolowany przez wysoki poziom RANTES/FGF-2. W rezultacie, aby postawić diagnozę, Lechner i von Baehr sugerują zmniejszenie nacisku na obecność stanu zapalnego i rozważenie szlaku sygnalizacyjnego, głównie poprzez nadekspresję RANTES/FGF-2. Wysoki poziom RANTES/FGF-2 u pacjentów z kawitacją wskazuje, że zmiany te mogą powodować podobne i wzajemnie wzmacniające się patogenne szlaki sygnałowe do innych narządów. Układ odpornościowy jest aktywowany w odpowiedzi na sygnały zagrożenia, które wywołują różne wrodzone szlaki molekularne, których kulminacją jest produkcja cytokin zapalnych i możliwa aktywacja nabytego układu odpornościowego. Potwierdza to ideę i teorię, że kawitacja kości szczęki może służyć jako podstawowa przyczyna przewlekłych chorób zapalnych poprzez wytwarzanie RANTES/FGF-2, a także wyjaśnia, dlaczego ostre objawy zapalenia nie zawsze są widoczne lub odczuwane przez pacjenta w zmianach w kości szczęki sobie. Zatem ubytki kości szczęki i związane z nimi przekaźniki stanowią integracyjny aspekt choroby zapalnej i służą jako potencjalna etiologia choroby. Usunięcie kawitacji może być kluczem do cofnięcia chorób zapalnych. Potwierdza to obserwacja zmniejszenia poziomu RANTES w surowicy po interwencji chirurgicznej u 5 pacjentek z rakiem piersi (patrz Tabela 5). Dalsze badania i testowanie poziomów RANTES/CCL5 mogą dostarczyć wglądu w tę zależność. Zachęcającymi obserwacjami jest poprawa jakości życia wielu pacjentów z kawitacją kości szczęki, niezależnie od tego, czy chodzi o ulgę w miejscu operacji, czy zmniejszenie przewlekłego stanu zapalnego lub choroby w innym miejscu.
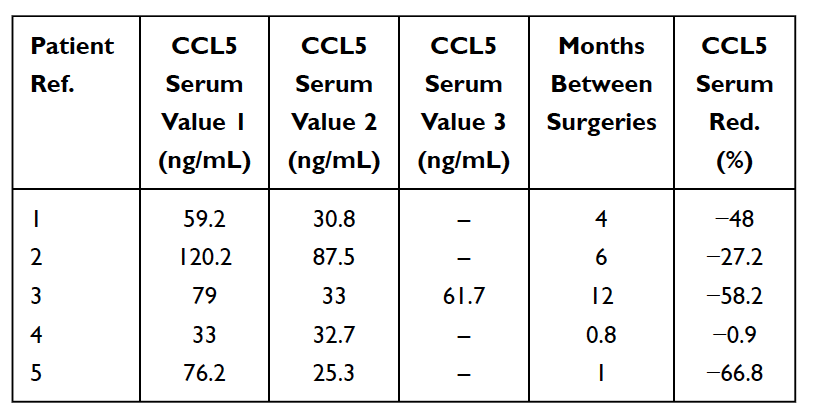
Tabela 5
Zmniejszenie (red.) RANTES/CCL5 w surowicy u 5 pacjentek z rakiem piersi, które przeszły operację z powodu tłuszczowo-zwyrodnieniowej martwicy kości szczęki (FDOJ). Stół zaadaptowany z
Lechner i wsp., 2021. Kawitacja kości szczęki wyrażona RANTES/CCL5: Studia przypadków łączące ciche zapalenie kości szczęki z epistemologią raka piersi”. Rak piersi: cele i terapia.
Ze względu na niedostatek literatury na temat leczenia uszkodzeń kawitacyjnych IAOMT przeprowadziła ankietę wśród swoich członków, aby zebrać informacje na temat trendów i sposobów leczenia zmierzających do osiągnięcia „standardu opieki”. Wyniki badania zostały pokrótce omówione w Załączniku II.
Po ustaleniu lokalizacji i wielkości zmian konieczne jest określenie sposobów leczenia. IAOMT stoi na stanowisku, że ogólnie niedopuszczalne jest pozostawianie „martwych kości” w organizmie człowieka. Opiera się to na danych sugerujących, że kawitacje kości szczęki mogą być ogniskami ogólnoustrojowych cytokin i endotoksyn, które rozpoczynają proces pogarszania ogólnego stanu zdrowia pacjenta.
W idealnych okolicznościach należy wykonać biopsję, aby potwierdzić rozpoznanie jakiejkolwiek patologii kości szczęki i wykluczyć inne stany chorobowe. Następnie konieczne jest leczenie mające na celu usunięcie lub wyeliminowanie zajętej patologii i stymulację odrostu normalnej, żywotnej kości. Obecnie w recenzowanej literaturze preferowaną metodą leczenia ubytków kości szczęki jest leczenie chirurgiczne polegające na wycięciu dotkniętej, martwej kości. Leczenie wymaga stosowania miejscowych środków znieczulających, co prowadzi do ważnej kwestii. Wcześniej sądzono, że u pacjentów, u których mogło wystąpić już upośledzenie przepływu krwi związane ze stanem chorobowym, należy unikać środków znieczulających zawierających epinefrynę, które mają znane właściwości zwężające naczynia krwionośne. Jednakże w serii badań molekularnych wykazano, że zróżnicowanie osteoblastów wzrosło po zastosowaniu epinefryny. Dlatego klinicysta musi w każdym przypadku indywidualnie określić, czy zastosować epinefrynę, a jeśli tak, to w jakiej ilości, która zapewni najlepsze wyniki.
Po chirurgicznym odkorkowaniu i dokładnym łyżeczkowaniu zmiany oraz płukaniu sterylnym roztworem soli fizjologicznej, gojenie jest wspomagane poprzez umieszczenie w pustce kostnej przeszczepów fibryny bogatopłytkowej (PRF). Stosowanie koncentratów fibryny bogatopłytkowej w zabiegach chirurgicznych jest korzystne nie tylko z punktu widzenia krzepnięcia, ale także uwalniania czynników wzrostu w okresie do czternastu dni po zabiegu. Przed zastosowaniem przeszczepów PRF i innych terapii wspomagających nawrót zmian osteonekrotycznych kości szczęki po operacji występował aż u 40% przypadków.
Analiza zewnętrznych czynników ryzyka przedstawionych w Tabeli 2 zdecydowanie sugeruje, że niekorzystnych wyników można uniknąć dzięki odpowiedniej technice chirurgicznej i interakcji lekarz-pacjent, zwłaszcza w podatnych populacjach. Wskazane jest rozważenie zastosowania technik atraumatycznych, minimalizacji lub zapobiegania chorobom przyzębia i innych zębów oraz wybór takiego arsenału, który pozwoli uzyskać najlepsze efekty gojenia. Zapewnienie pacjentowi dokładnych instrukcji przed i pooperacyjnych, w tym dotyczących zagrożeń związanych z paleniem papierosów, może pomóc zminimalizować negatywne skutki.
Mając na uwadze szeroką listę potencjalnych czynników ryzyka wymienioną w tabelach 2 i 3, zaleca się konsultację z zespołem opieki rozszerzonej nad pacjentem w celu prawidłowego ustalenia ewentualnych ukrytych czynników ryzyka, które mogą przyczyniać się do rozwoju kawitacji kości szczęki. Na przykład ważną kwestią podczas leczenia ubytków kości szczęki jest to, czy dana osoba przyjmuje leki przeciwdepresyjne, w szczególności selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI). Stosowanie SSRI wiąże się ze zmniejszoną gęstością masy kostnej i zwiększoną częstością złamań. Fluoksetyna SSRI (Prozac) bezpośrednio hamuje różnicowanie i mineralizację osteoblastów. Co najmniej dwa niezależne badania porównujące użytkowników SSRI z grupą kontrolną wykazały, że stosowanie SRRI wiąże się z gorszymi panoramicznymi wskaźnikami morfometrycznymi.
Przygotowanie wstępne może również przyczynić się do pomyślnych wyników leczenia. Polega to na stworzeniu środowiska tkankowego sprzyjającego gojeniu poprzez dostarczenie organizmowi odpowiedniego poziomu odpowiednich składników odżywczych, które poprawiają teren biologiczny poprzez optymalizację homeostazy w organizmie. Taktyki wstępnego przygotowania nie zawsze są możliwe lub akceptowalne przez pacjenta, ale są ważniejsze w przypadku pacjentów, u których występują pewne podatności, na przykład u pacjentów z predyspozycjami genetycznymi, zaburzeniami gojenia się lub osłabionym stanem zdrowia. W takich przypadkach niezwykle ważne jest, aby optymalizacja ta miała na celu zminimalizowanie poziomu stresu oksydacyjnego, który może nie tylko stymulować proces chorobowy, ale także zakłócać pożądane gojenie.
Idealnie byłoby, gdyby przed leczeniem ubytków kości szczęki całkowicie usunięto toksyczne obciążenie organizmu, takie jak fluor i/lub rtęć z wypełnień amalgamatowych. Rtęć może wypierać żelazo w łańcuchu transportu elektronów w mitochondriach. Powoduje to nadmiar wolnego żelaza (żelazawego lub Fe++), wytwarzającego szkodliwe reaktywne formy tlenu (ROS), znane również jako wolne rodniki, które powodują stres oksydacyjny. Nadmiar żelaza w tkance kostnej hamuje także prawidłowe funkcjonowanie osteoblastów, co oczywiście będzie miało negatywny wpływ na leczenie schorzeń kości.
Przed leczeniem należy również uzupełnić inne braki. Kiedy występuje niedobór biodostępnej miedzi, magnezu i retinolu, metabolizm i recykling żelaza ulegają rozregulowaniu w organizmie, co przyczynia się do gromadzenia nadmiaru wolnego żelaza w niewłaściwych miejscach, co prowadzi do jeszcze większego stresu oksydacyjnego i ryzyka chorób. Mówiąc dokładniej, wiele enzymów w organizmie (takich jak ceruloplazmina) staje się nieaktywnych, gdy poziom biodostępnej miedzi, magnezu i retinolu jest niewystarczający, co z kolei utrwala ogólnoustrojową dysregulację poziomu żelaza i wynikający z tego wzrost stresu oksydacyjnego i ryzyka chorób.
Alternatywne strategie leczenia
Należy również ocenić alternatywne techniki stosowane jako terapie podstawowe lub wspomagające. Należą do nich homeopatia, stymulacja elektryczna, terapia światłem, taka jak fotobiomodulacja i laser, tlen/ozon klasy medycznej, tlen hiperbaryczny, metody przeciwzakrzepowe, środki Sanum, odżywianie i nutraceutyki, sauna na podczerwień, dożylna terapia ozonem, terapie energetyczne i inne. W chwili obecnej nie przeprowadzono badań, które potwierdzałyby skuteczność lub nieskuteczność tych alternatywnych form leczenia. Należy ustalić standardy opieki zapewniające prawidłowe gojenie i detoksykację. Należy przetestować i ujednolicić techniki oceny sukcesu. Do oceny należy przedstawić protokoły lub procedury pomagające określić, kiedy leczenie jest właściwe, a kiedy nie.
Badania wykazały, że występowanie kawitacji kości szczęki jest podstępnym procesem chorobowym związanym ze zmniejszonym przepływem krwi. Zaburzony szpikowy przepływ krwi prowadzi do słabo zmineralizowanego i niewystarczającego unaczynienia w obszarach kości szczęki, które mogą zostać zakażone patogenami, zwiększając śmierć komórek. Powolny przepływ krwi w obrębie zmian kawitacyjnych utrudnia dostarczanie antybiotyków, składników odżywczych i przekaźników odpornościowych. Środowisko niedokrwienne może również zawierać i promować mediatory przewlekłego stanu zapalnego, które mogą mieć jeszcze bardziej szkodliwy wpływ na zdrowie ogólnoustrojowe. Predyspozycje genetyczne, obniżona odporność, skutki niektórych leków, urazy i infekcje oraz inne czynniki, takie jak palenie, mogą powodować lub przyspieszać rozwój kawitacji kości szczęki.
Wraz z wybitnym patologiem kości szczęki, dr Jerrym Bouquot, IAOMT prezentuje i promuje histologicznie i patologicznie prawidłową identyfikację uszkodzeń kawitacyjnych kości szczęki jako przewlekłą niedokrwienną chorobę rdzeniastą kości szczęki, CIMDJ. Chociaż w przeszłości i obecnie używa się wielu nazw, akronimów i terminów do określenia tej choroby, IAOMT jest przekonane, że jest to najwłaściwszy termin do opisania stanu patologicznego i mikrohistologicznego powszechnie spotykanego w przypadku kawitacji kości szczęki.
Chociaż większość zmian kawitacyjnych kości szczęki jest trudna do zdiagnozowania na podstawie rutynowych zdjęć rentgenowskich i większość z nich nie jest bolesna, nigdy nie należy zakładać, że proces chorobowy nie istnieje. Istnieje wiele procesów chorobowych, które są trudne do zdiagnozowania i wiele, które nie są bolesne. Gdybyśmy uznali ból za wskaźnik leczenia, choroby przyzębia, cukrzyca i większość nowotworów pozostałyby nieleczone. Dzisiejszy lekarz dentysta dysponuje szerokim spektrum metod skutecznego leczenia ubytków kości szczęki, a brak rozpoznania choroby i zalecenia leczenia jest nie mniej poważny niż brak diagnozy i leczenia chorób przyzębia. Dla zdrowia i dobrego samopoczucia naszych pacjentów kluczowa jest zmiana paradygmatu dla wszystkich pracowników służby zdrowia, w tym lekarzy dentystów i lekarzy, aby 1) rozpoznali częstość występowania ubytków kości szczęki oraz 2) uznali związek między ubytkami kości szczęki a chorobami ogólnoustrojowymi.
WYNIKI BADANIA IAOMT 2 (2023)
Jak pokrótce omówiono w artykule, niepowiązane ze sobą schorzenia często ustępują po operacji kawitacyjnej. Aby dowiedzieć się więcej o tym, jakie rodzaje schorzeń ustępują i jak następuje proksymalna remisja w związku z operacją, do członków IAOMT wysłano drugą ankietę. Na potrzeby ankiety sporządzono listę objawów i schorzeń, które według członków tej komisji uległy poprawie po operacji. Respondentów zapytano, czy zaobserwowali ustąpienie któregokolwiek z tych schorzeń po operacji i jeśli tak, w jakim stopniu. Zapytano ich również, czy objawy szybko ustąpiły, czy też poprawa trwała dłużej niż dwa miesiące. Ponadto respondentów pytano, czy zazwyczaj przeprowadzają operacje w pojedynczych miejscach, w wielu jednostronnych lokalizacjach, czy też we wszystkich miejscach w ramach jednego zabiegu. Wyniki badania przedstawiono na wykresach poniżej. Dane mają charakter wstępny, biorąc pod uwagę niewielką liczbę respondentów (33) i brak niektórych danych.
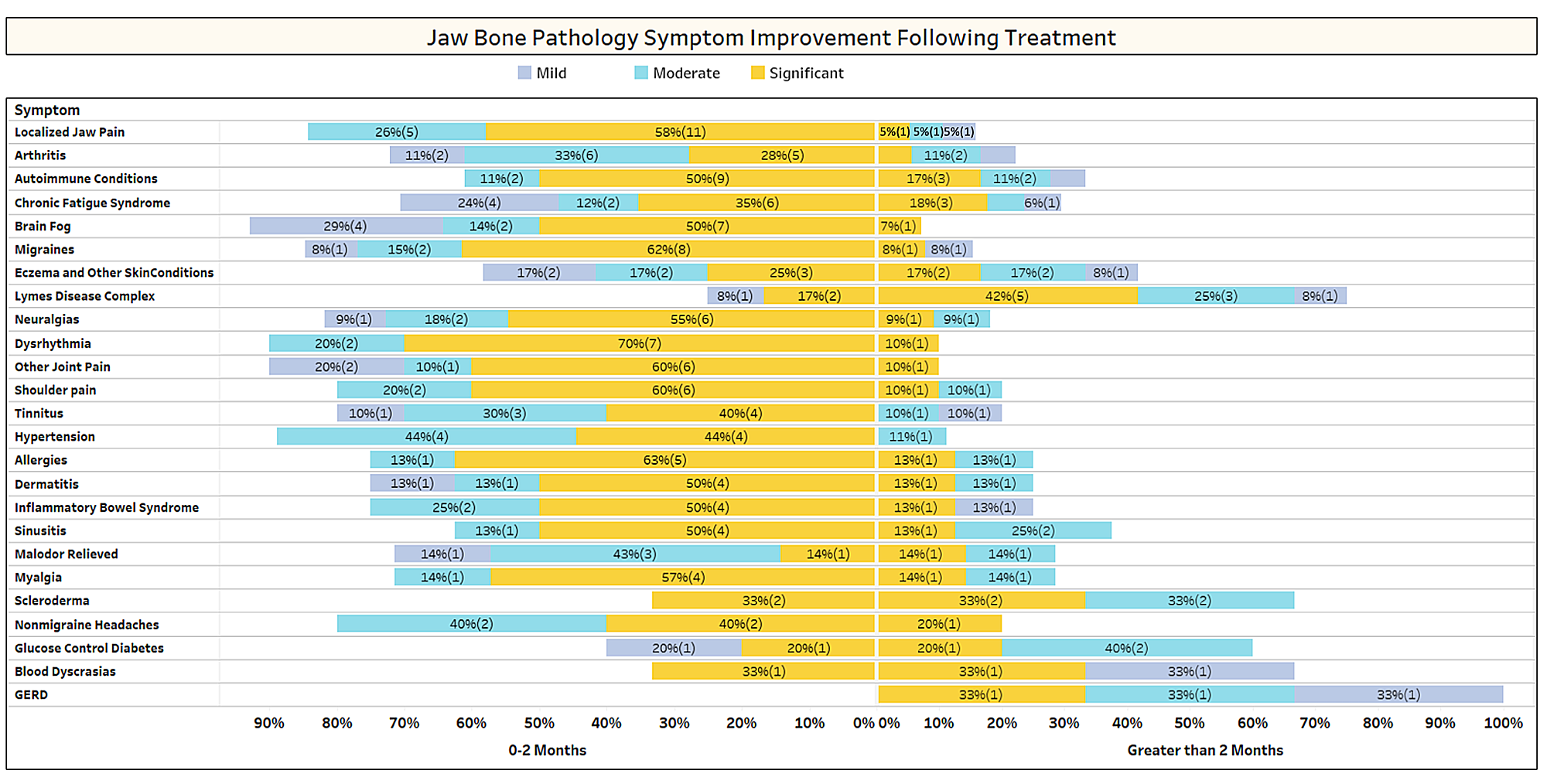
Załącznik I Ryc. 1 Respondenci oceniali poziom poprawy (łagodny, umiarkowany lub znaczący) i zaznaczali, czy poprawa nastąpiła szybko (0-2 miesiące), czy też trwała dłużej (> 2 miesiące). Stany/objawy wymieniono w kolejności najczęściej zgłaszanych. Należy pamiętać, że większość schorzeń/objawów ustępuje w czasie krótszym niż dwa miesiące (lewa strona linii środkowej).
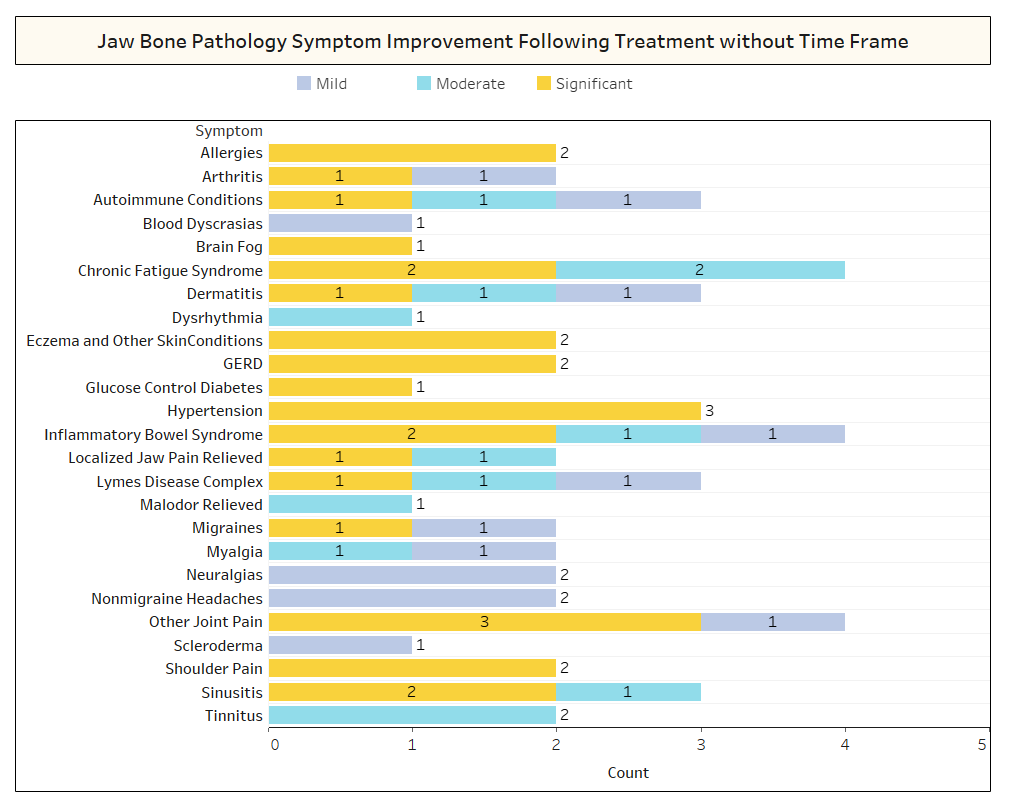
Załącznik I Ryc. 2 Jak pokazano powyżej, w kilku przypadkach Respondenci nie odnotowali ram czasowych powrotu do zdrowia w odniesieniu do zaobserwowanej poprawy.
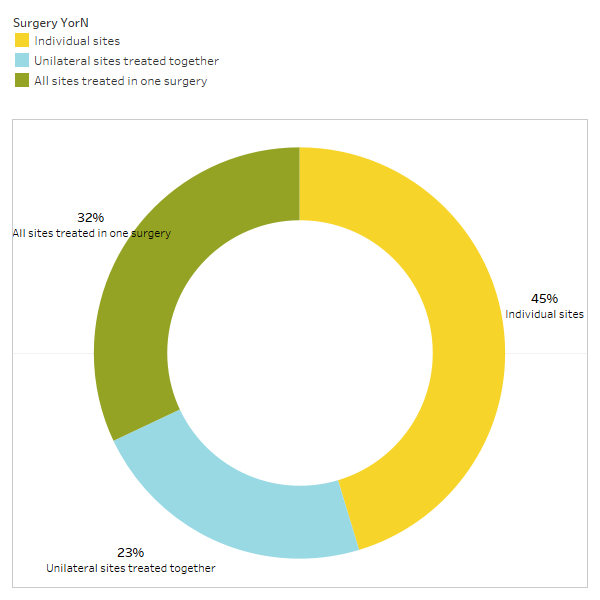
Załącznik I Ryc. 3 Respondenci odpowiadali na pytanie: „Czy zazwyczaj polecasz/wykonujesz
operacja pojedynczych miejsc, jednostronne miejsca leczone razem czy wszystkie miejsca leczone w ramach jednej operacji?”
WYNIKI BADANIA IAOMT 1 (2021)
Ze względu na niedostatek literatury i przeglądów przypadków klinicznych dotyczących leczenia uszkodzeń kawitacyjnych, IAOMT przeprowadziła ankietę wśród swoich członków, aby zebrać informacje na temat trendów i sposobów leczenia zmierzających do „standardu opieki”. Pełna ankieta jest dostępna na stronie internetowej IAOMT (należy pamiętać, że nie wszyscy praktycy odpowiedzieli na wszystkie pytania zawarte w ankiecie).
Podsumowując, większość z 79 respondentów oferuje leczenie chirurgiczne, które obejmuje odbicie tkanek miękkich, dostęp chirurgiczny do miejsca kawitacji oraz różne metody fizycznego „oczyszczenia” i dezynfekcji zajętego miejsca. W celu przyspieszenia gojenia zmiany chorobowej przed zamknięciem nacięcia tkanki miękkiej stosuje się szeroką gamę leków, nutraceutyków i/lub produktów krwiopochodnych.
Aby otworzyć lub uzyskać dostęp do zmiany kostnej, często stosuje się wiertła obrotowe. Większość klinicystów używa ręcznego narzędzia do kiretowania lub zeskrobywania chorej kości (68%), ale stosowane są również inne techniki i narzędzia, takie jak wiertło obrotowe (40%), instrument piezoelektryczny (ultradźwiękowy) (35%) lub Laser ER:YAG (36%), czyli częstotliwość lasera wykorzystywana do strumieniowania fotoakustycznego.
Po oczyszczeniu, oczyszczeniu i/lub wyleczeniu rany, większość respondentów używa wody/gazu ozonowego do dezynfekcji i wspomagania gojenia. 86% ankietowanych stosuje PRF (fibrynę bogatopłytkową), PRP (osocze bogatopłytkowe) lub ozonowane PRF lub PRP. Obiecującą techniką dezynfekcji opisaną w literaturze iw tym badaniu (42%) jest śródoperacyjne zastosowanie Er:YAG. 32% ankietowanych nie wykorzystuje żadnego rodzaju przeszczepu kostnego do wypełnienia miejsca kawitacji.
Większość respondentów (59%) zazwyczaj nie wykonuje biopsji zmian, podając różne przyczyny, takie jak koszt, niemożność uzyskania żywych próbek tkanek, trudności ze znalezieniem laboratorium patologicznego lub pewność statusu choroby.
Większość respondentów nie stosuje antybiotyków przedoperacyjnie (79%), w trakcie operacji (95%) i pooperacyjnie (69%). Inne stosowane środki dożylne obejmują steroidy deksametazonu (8%) i witaminę C (48%). Wielu respondentów (52%) wykorzystuje pooperacyjną terapię laserem niskoenergetycznym (LLLT) w celach leczniczych. Wielu respondentów zaleca wsparcie żywieniowe, w tym witaminy, minerały i różne leki homeopatyczne przed (81%) i w trakcie (93%) okresu gojenia.
 Obrazy
Obrazy
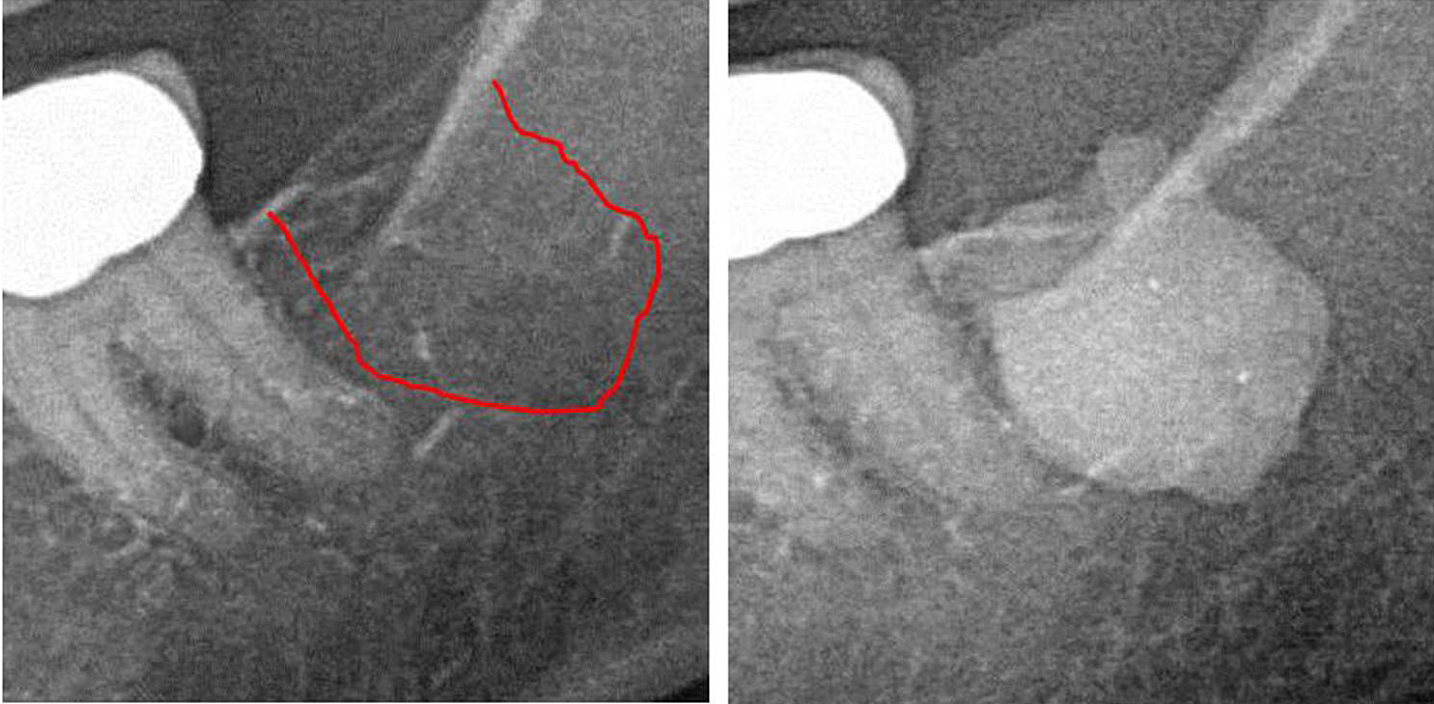
Załącznik III Ryc. 1 Lewy panel: diagnostyka rentgenowska 2D obszaru nr 38. Panel prawy: Dokumentacja rozległości FDO) w okolicy zatrzonowcowej 38/39 z zastosowaniem środka kontrastowego po operacji FDOJ.
Skróty: FDOJ, tłuszczowa zwyrodnieniowa martwica kości szczęki.
Na podstawie: Lechner i wsp., 2021. „Kawitacja kości szczęki wyrażona w RANTES/CCL5: studia przypadków łączące ciche zapalenie kości szczęki z epistemologią raka piersi”. Rak piersi: cele i terapia
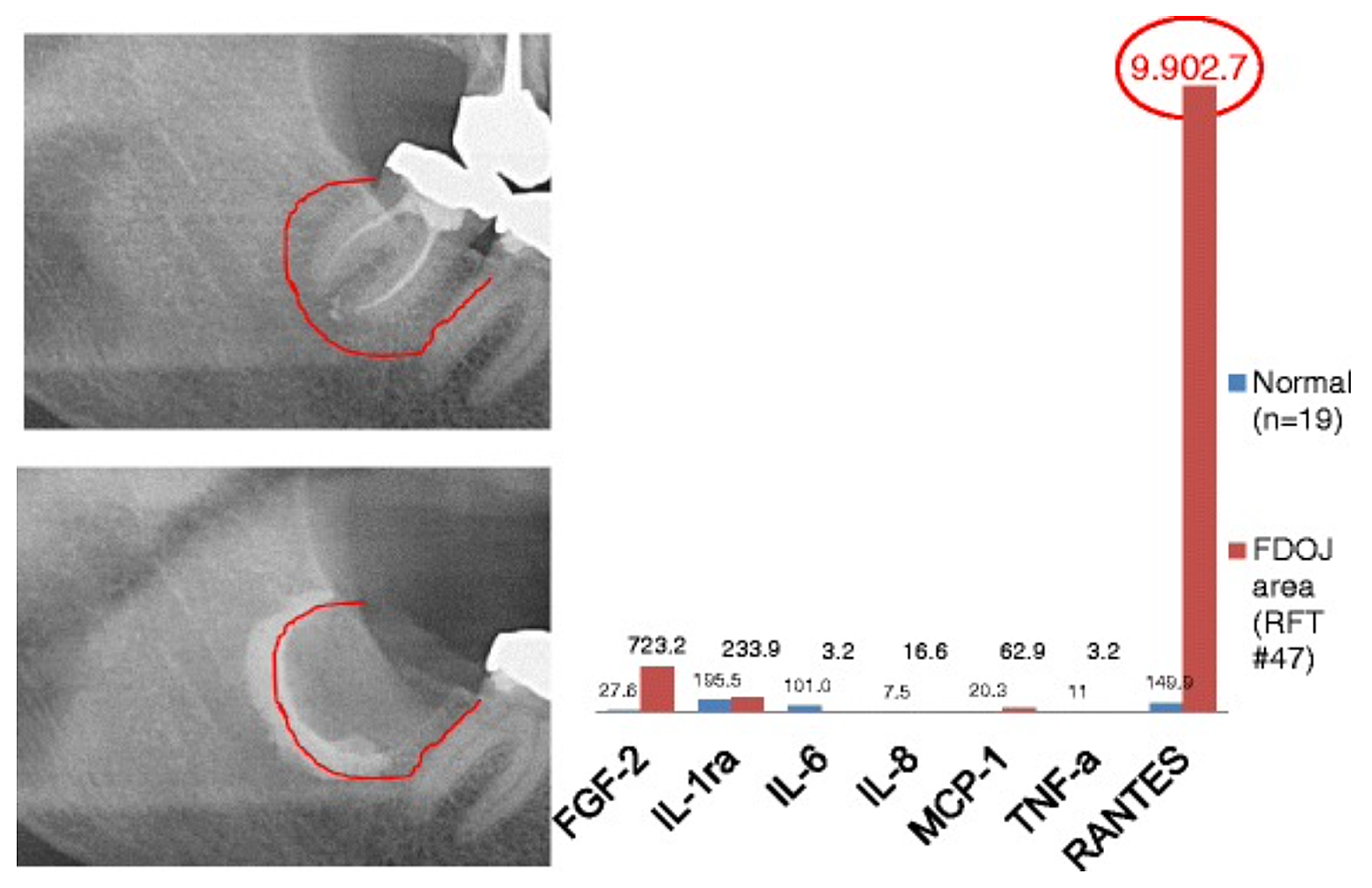
Załącznik 3 Ryc. 2 Porównanie siedmiu cytokin (FGF-2, IL-1ra, IL-6, IL-8, MCP-1, TNF-a i RANTES) w FDOJ pod RFT #47 z cytokinami w zdrowej kości szczęki (n = 19). Śródoperacyjna dokumentacja przedłużenia FDOJ w prawej dolnej szczęce, obszar #47, wierzchołkowo RFT #47, przy użyciu środka kontrastowego po chirurgicznym usunięciu RFT #47.
Skróty: FDOJ, tłuszczowa zwyrodnieniowa martwica kości szczęki.
Na podstawie: Lechner i von Baehr, 2015. „Chemokina RANTES/CCL5 jako nieznany związek między gojeniem się ran w kości szczęki a chorobami ogólnoustrojowymi: czy przewidywanie i dostosowane leczenie są na horyzoncie?” Dziennik EPMA
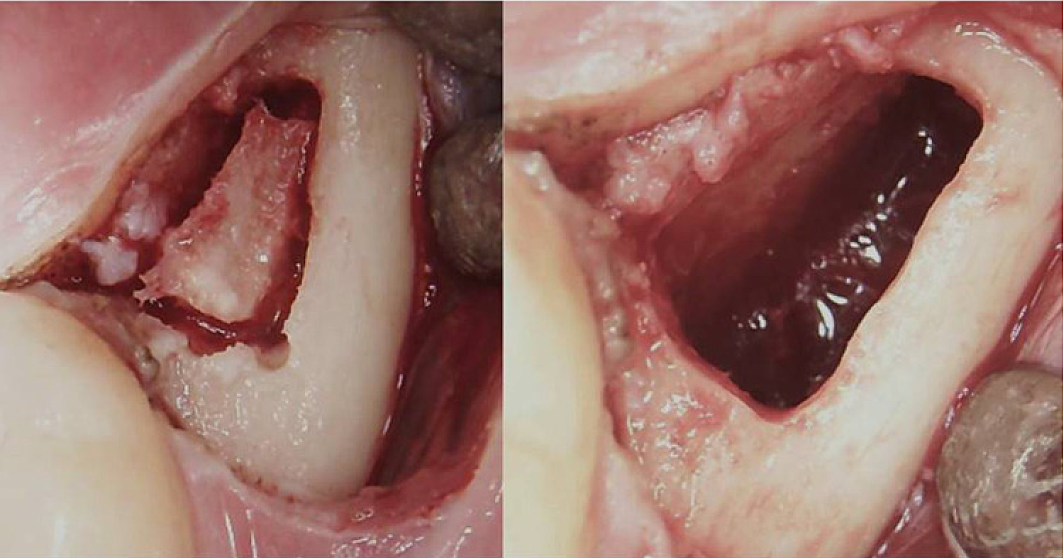
Załącznik III Ryc. 3 Zabieg chirurgiczny w przypadku retromolarnego BMDJ/FDOJ. Panel lewy: po załamaniu płata śluzówkowo-okostnowego w korze mózgowej uformowało się okienko kostne. Panel prawy: wyleczona jama szpikowa.
Skróty: BMDJ, ubytek szpiku kostnego w kości szczęki; FDOJ, tłuszczowa zwyrodnieniowa martwica kości szczęki.
Na podstawie: Lechner i wsp., 2021. „Zespół chronicznego zmęczenia i wady szpiku kostnego szczęki – opis przypadku dotyczący dodatkowej diagnostyki rentgenowskiej zębów za pomocą ultradźwięków”. Międzynarodowy Dziennik Sprawozdań Medycznych
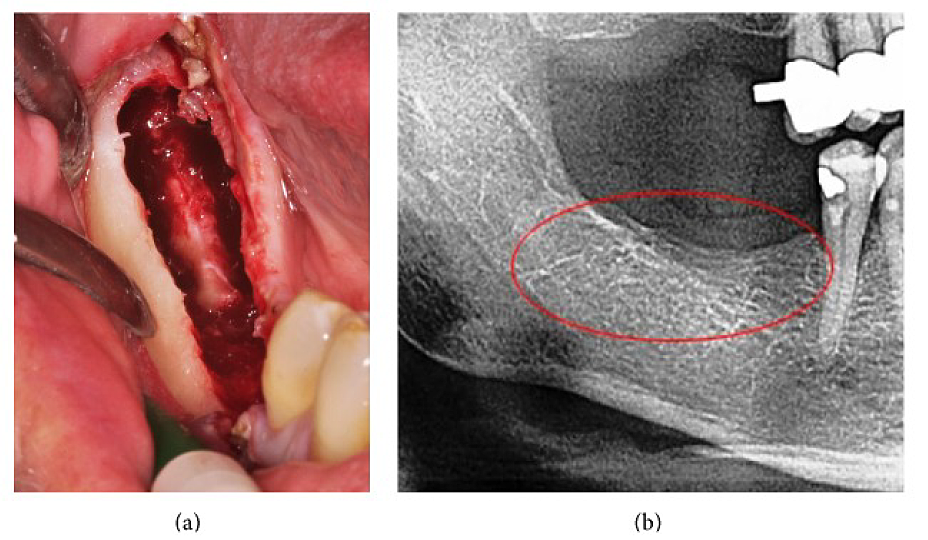
Załącznik III Ryc. 4 (a) Łyżeczkowanie FDOJ w żuchwie z obnażonym nerwem podzębodołowym. (b) Odpowiednie zdjęcie rentgenowskie bez cech procesu patologicznego w kości szczęki.
Skróty: FDOJ, tłuszczowa zwyrodnieniowa martwica kości szczęki
Na podstawie: Lechner i in., 2015. „Obwodowy neuropatyczny ból twarzy/trójdzielca i RANTES/CCL5 w kawitacji kości szczęki”. Oparta na dowodach komplementarna i alternatywna medycyna
Dodatek III Film 1
Film wideo (kliknij dwukrotnie na obrazek, aby obejrzeć klip) przedstawiający operację kości szczęki przedstawiający kuleczki tłuszczu i ropną wydzielinę z kości szczęki u pacjenta, u którego podejrzewano martwicę kości szczęki. Dzięki uprzejmości dr Miguela Stanleya, DDS
Dodatek III Film 2
Film wideo (kliknij dwukrotnie na obrazek, aby obejrzeć klip) przedstawiający operację kości szczęki przedstawiający kuleczki tłuszczu i ropną wydzielinę z kości szczęki u pacjenta, u którego podejrzewano martwicę kości szczęki. Dzięki uprzejmości dr Miguela Stanleya, DDS
Aby pobrać lub wydrukować tę stronę w innym języku, wybierz najpierw swój język z menu rozwijanego w lewym górnym rogu.
Stanowisko IAOMT w sprawie autorów kawitacji ludzkiej kości szczęki













